1. 研究背景
生命体内核糖体翻译均以N→C方向延伸肽链,但经典前生命模拟(干-湿循环、热聚合或羧基活化)只能产生无序寡肽(图1),无法解释“氨基端→羧基端”这一通用方向性的化学起源;同时,水溶液中氨基酸缩合热力学不利、无酶条件下缺乏定向活化-选择机制,成为“氨基酸→蛋白质”链条中的重要缺口。
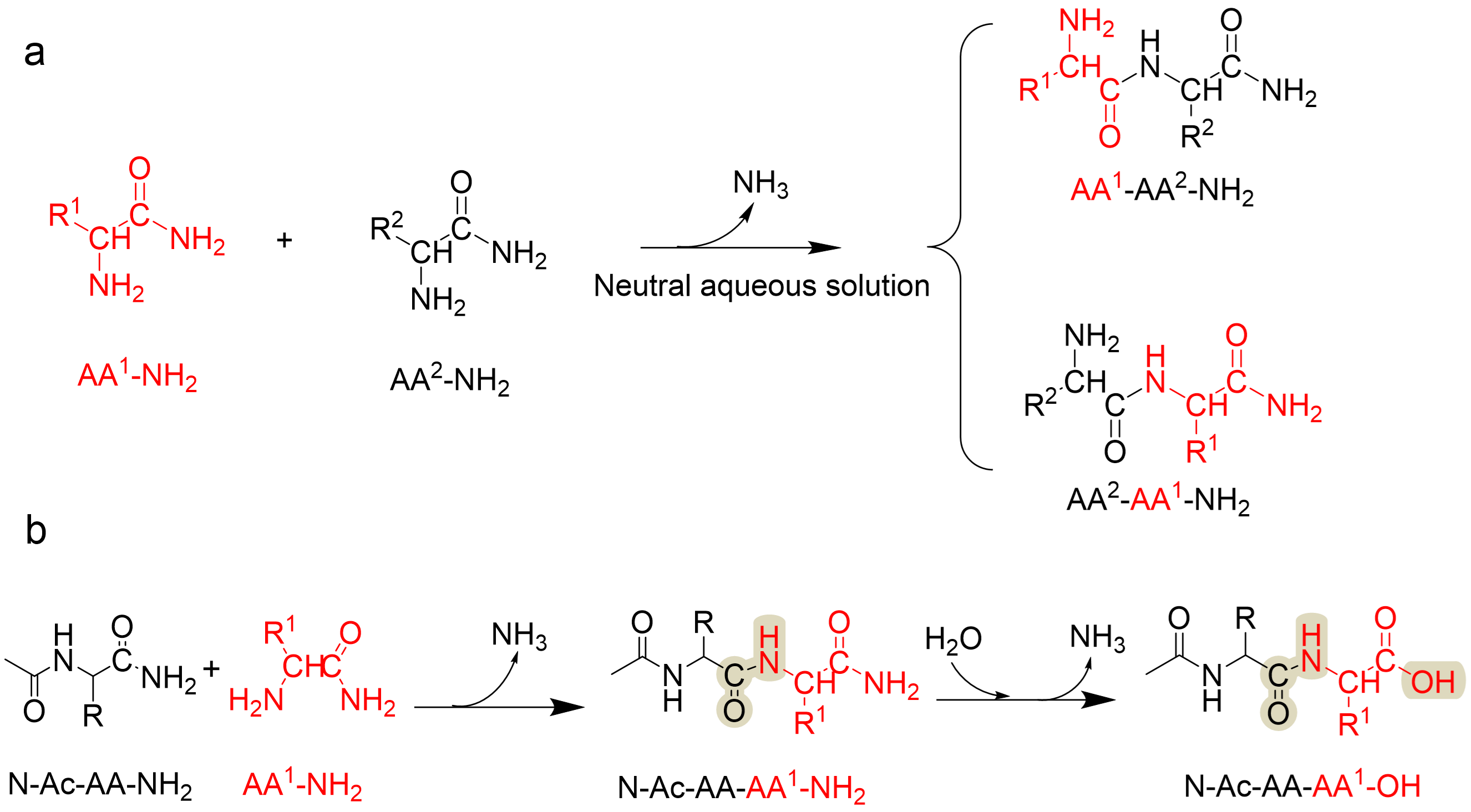
图1 氨基酸酰胺的聚合反应。(a)AA-NH2 自身的反应。(b)Ac-AA-NH2 与 AA-NH2 的反应。
2. N-to-C前生命肽的聚合
在真核蛋白的各种化学修饰中,N-乙酰化是最常见的修饰之一。类似地,在原核生物中第一个氨基酸的N端也观察到了类似的化学修饰。氨基酸酰胺(AA-NH2)被认为是前生命阶段潜在的衍生物之一,将氨基酸酰胺进行N-乙酰化修饰,利用乙酰化氨基酸酰胺作为肽链的初始N端,氨基酸酰胺作为延伸底物,通过简单的干湿循环反应,实现了从N端到C端的前生命肽合成(图1),无需使用任何激活剂,并且检测到最高十聚体的产物。此外,随后进行的31个独立实验证实了肽链N→C方向延伸的可行性。结果表明,各种AA-NH2的不同侧链分子在与N-Ac-AA-NH2聚合时表现出不同的性质,导致所产生的聚合物在长度上存在差异。总之,本研究基于氨基酸酰胺的反应,在前生命条件下构建了一个可行的肽类N to C端延伸模型。我们推测,该模型可能是一个“分子化石”,代表了现存生物肽合成方式的可能前生命演化途径。
成果发表于国际学术期刊Chemical Communications(张丽,张敏,郭笑汎,甘定伟,叶勇,赵玉芬,应见喜*. A model for N-to-C direction in prebiotic peptide synthesis [J]. Chemical Communications, 2024, 60, 2748-2751. DOI: 10.1039/D3CC06101A.)。
附件:

