同手性是生命系统中的一个核心特征,是指生物体内所有蛋白质均由L-氨基酸构成,而核酸则由D-核糖或D-脱氧核糖构成。这种手性特征被认为是生命的标志之一,也是生物分子稳定性和功能的基础。然而,早期地球中L-氨基酸和D-氨基酸的比例接近1:1,在没有现代酶系统的环境中,如何产生同手性分子、克服L-和D-氨基酸的对称性,形成稳定的生物大分子,仍是一个悬而未解的谜。
近几年来,科学家们提出了许多假设和机制,尝试解释早期地球上同手性分子的来源,如矿物表面吸附、磁场效应及对称性破坏等。尽管这些机制大多涉及特定的物理过程,生命起源和演化仍是物理、化学和生物因素复杂相互作用的结果。生物体内,肽的合成过程依赖于5’-aa-AMP这一活性中间体,因此,作为5’-aa-AMP潜在前生物前体的N-aa-AMP,在与氨基酸结合产生肽的过程中是否具有手性选择性,成为了一个亟待探讨的重要问题。
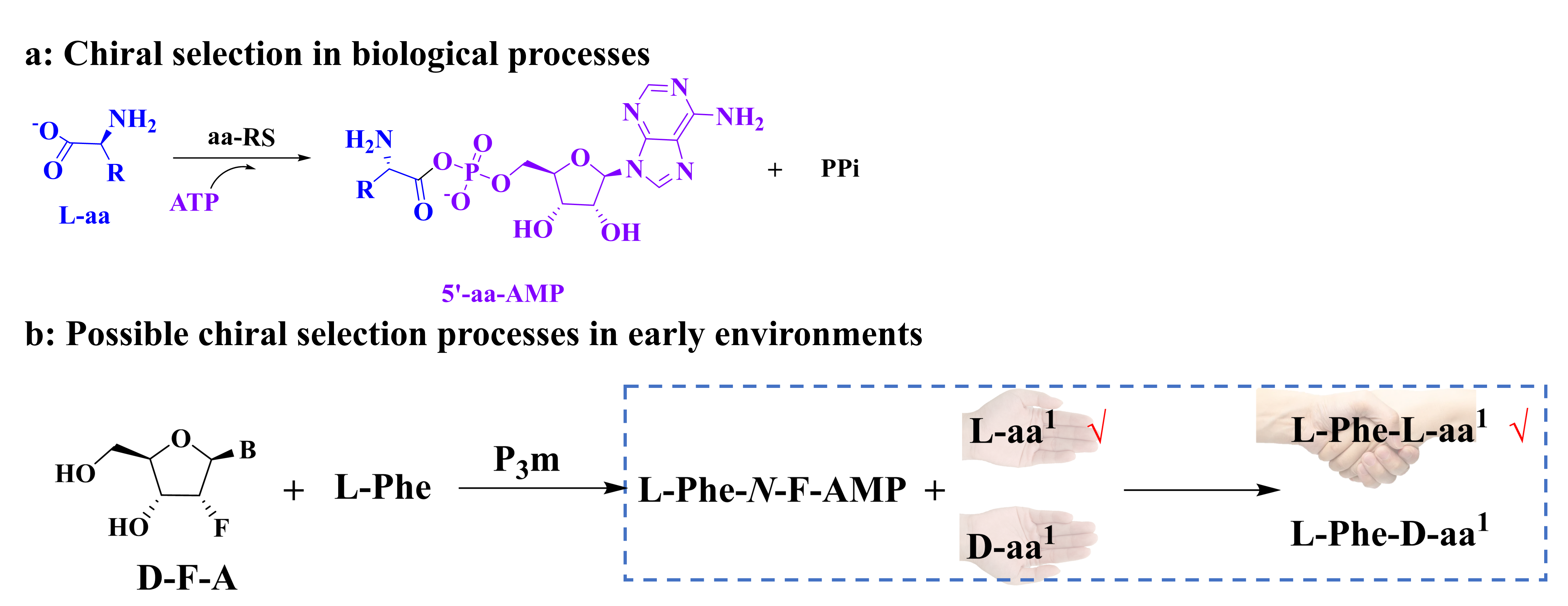
图1 (a) L-氨基酸和ATP形成5’-aa-AMP的生物合成途径。(b) 基于N-Phe-F-AMP的手性选择。其中符号“√”代表优选的手性结构。
宁波大学新药技术研究院的研究生张敏与应见喜研究员、赵玉芬教授等,受体内肽合成过程的启发,开展了基于N-aa-AMP的肽合成中手性选择的研究。
通过高效液相色谱-质谱联用(LC-MS)技术,我们对实验样品进行了分析。研究结果表明,在实验过程中,N-L-aa-AMP优先与L-氨基酸结合,而N-D-aa-AMP则偏好与D-氨基酸结合,从而有效促进了同手性肽的形成。在不同氨基酸的反应中,手性选择效应有所差异,特别是在异亮氨酸和脯氨酸中表现得更为明显。进一步的理论计算以异亮氨酸为例,表明L-氨基酸与N-L-aa-AMP反应时,转化能量壁垒较低,促进了L-氨基酸优先参与肽链合成。该研究为深入理解早期生命中同手性选择的机制提供了新的实验数据和理论支持,推动了生命起源中手性选择问题的进一步探讨。
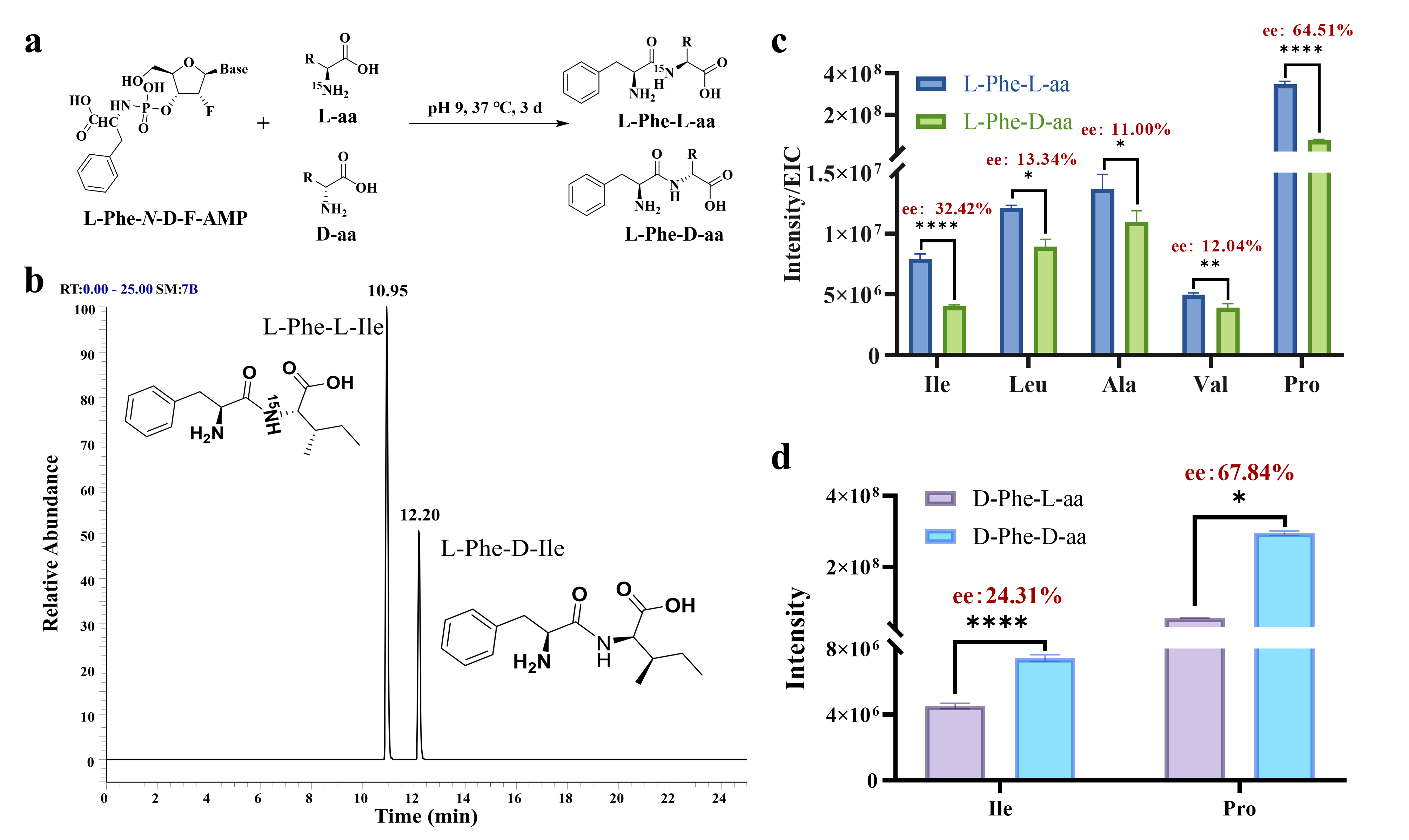 图2 (a)基于N-Phe-D-F-AMP合成不同的手性肽。(b)N-L-Phe-D-F-AMP与外消旋Ile反应产物的提取离子色谱图。(c) N-L-Phe-D-F-AMP与不同外消旋AA反应,产物中不同手性肽进行比较。(d) N-D-Phe-D-F-AMP与不同外消旋AA反应,产物中不同手性肽进行比较。****表示P值 < 0.0001,**表示P值 < 0.01,*表示P值 < 0.05。
图2 (a)基于N-Phe-D-F-AMP合成不同的手性肽。(b)N-L-Phe-D-F-AMP与外消旋Ile反应产物的提取离子色谱图。(c) N-L-Phe-D-F-AMP与不同外消旋AA反应,产物中不同手性肽进行比较。(d) N-D-Phe-D-F-AMP与不同外消旋AA反应,产物中不同手性肽进行比较。****表示P值 < 0.0001,**表示P值 < 0.01,*表示P值 < 0.05。
研究成果发表在学术期刊Chemical Communications(张敏,王守军,张丽,郭笑汎,甘定伟,孙冬茹,赵玉芬*,应见喜*. Biomimetic prebiotic synthesis of homochiral peptides via a potential 5’-aa-AMP precursor [J]. Chemical Communications, 2025, 61(7): 1375-1378. DOI:10.1039/d4cc05580b.)。研究受国家自然科学基金资助。
附件:

