基于铁蛋白纳米颗粒的肿瘤成像及药物靶向递送系统
纳米颗粒凭借其小尺寸、高比表面积、易修饰等特性在靶向治疗、分子影像、早期诊断和药物递送等方面可发挥着重要作用。作为新型的造影剂和药物载体,纳米颗粒未来将广泛应用于肿瘤的成像和治疗。但纳米颗粒用于肿瘤成像诊断及药物递送仍面临一些挑战,如在生物环境下的稳定性,对机体的安全性以及对肿瘤的靶向性和有效性等问题。因此,研发生物相容性好、安全性高和肿瘤靶向性显著的纳米颗粒成像和药物递送系统至关重要。
铁蛋白是一类广泛存在于有机体中的铁储存球形蛋白,由24个亚基组装而成,外部直径12纳米,内部空腔直径8纳米。其笼状结构使其具有很好的热稳定性和化学稳定性,易于使用化学或基因工程的方法对其进行修饰。人H亚基铁蛋白(HFn)已被证实能够与多种类型肿瘤表面表达的转铁蛋白受体1(TfR1)结合,展现出其主动靶向富集于肿瘤的特性,并且在应用到机体后免疫反应及毒性都较低,已显示出巨大的应用潜力。近年来,地球与行星物理院重点实验室地磁场与生物圈演化学科组利用基因工程异源表达的HFn作为模板,建立了基于该模板的仿生磁性纳米颗粒可控制备和修饰方法,在实验小鼠上成功地应用于肿瘤的核磁共振成像诊断、磁共振血管造影、肿瘤组织的可视化诊断等方面。最近,该学科组的蔡垚博士后与合作导师潘永信研究员又取得了如下研究进展:
1. 钆标记人H亚基铁蛋白作为T1造影剂用于肿瘤的磁共振成像
磁共振成像(MRI)是现代医学临床影像诊断中使用的一项重要技术,而MRI造影剂则是增强磁共振成像效果的关键环节。MRI造影剂按照作用原理可分为纵向弛豫(T1)造影剂和横向弛豫(T2)造影剂。目前临床上使用的T1磁共振造影剂主要为钆的复合物(Gd-DTPA)。但是基于钆的造影剂存在一定的缺陷,如引发肾源性系统性纤维化,在组织中沉积的风险以及较短的体内循环时间等。提高钆基造影剂的纵向弛豫率(r1),或增强钆基造影剂靶向肿瘤的能力,从而降低造影剂使用剂量是改善钆基造影剂效果和克服原有缺陷的有效途径。
蔡垚博士与合作者制备了新型HFn-Gd纳米颗粒。在7T磁共振仪器下测得r1值为4.78 mM-1 s-1,高于临床使用的商业Gd-DTPA(r1为3.97 mM-1 s-1)。通过细胞活性测试,砷偶氮比色法和激光扫描共聚焦显微镜检测显示出HFn-Gd具有良好的生物相容性,稳定性和对TfR1阳性癌细胞的主动靶向能力。在荷CFPAC-1肿瘤小鼠上单次注射HFn-Gd(剂量= 0.016 mmol Gd / kg体重,约为商业Gd-DTPA临床使用剂量的1/6)的 30分钟内显示出增强的MRI信号。HFn-Gd单次注射入荷MDA-MB-231微小肿瘤的小鼠尾静脉后,MRI表现出长达60分钟的显著信号变化,而商业Gd-DTPA在相同低的剂量下几乎没有可检测到的信号。此外, HFn-Gd纳米颗粒大部分通过肾脏系统清除。结果表明,HFn-Gd纳米颗粒有望成为用于肿瘤MRI检测的T1造影剂,避免使用高剂量的商业钆基造影剂带来潜在副作用的风险。
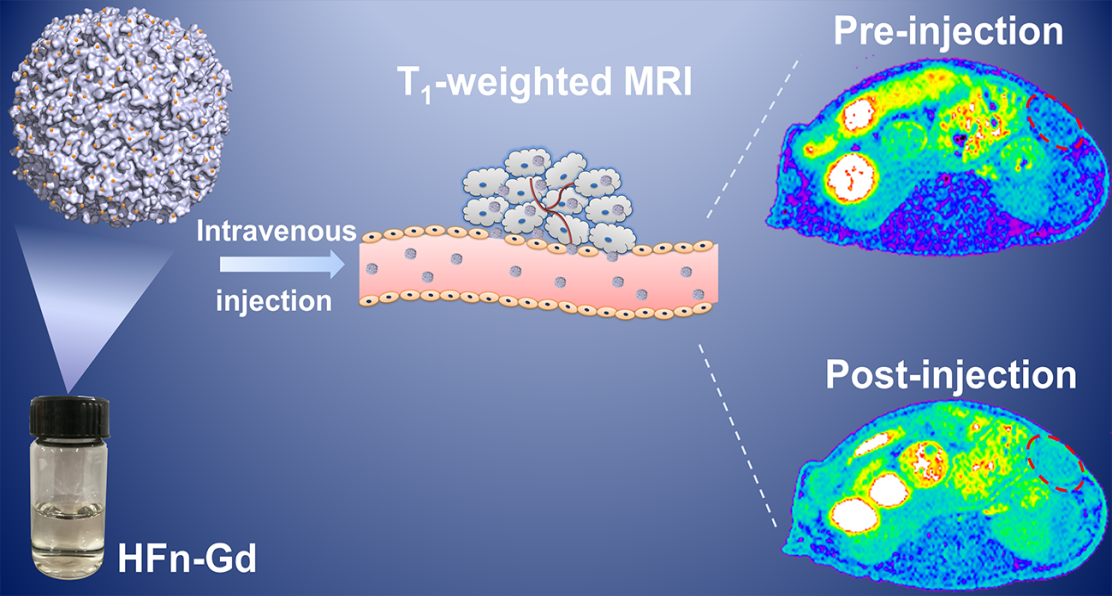
图1:钆标记人H亚基铁蛋白作为T1造影剂用于肿瘤的磁共振成像
该研究成果发表于Acs Applied Nano Materials上。Cai, Y., Wang, Y., Zhang, T., and Pan, Y. Gadolinium labeled ferritin nanoparticles as T1 contrast agents for magnetic resonance imaging of tumors. ACS Applied Nano Materials.2020,3(9),8771-8783. DOI: 10.1021/acsanm.0c01563.
2. 基于毕赤酵母表达人H亚基铁蛋白仿生合成磁性铁蛋白纳米颗粒
目前,HFn所使用的表达系统主要为大肠杆菌的原核蛋白表达系统,该表达系统下获得的蛋白在医学应用方面的劣势在于缺乏对真核生物蛋白质的复性功能、缺乏对真核生物蛋白质的修饰加工系统以及细胞周质内含有种类繁多的内毒素。巴斯德毕赤酵母表达系统是一种真核蛋白表达系统,由于其具有共翻译和翻译后修饰及与先进的真核表达系统的高度相似性,较低的培养成本,相对较快的重组蛋白表达时间及简化的蛋白质纯化工艺,已经较普遍的用于生产具有医学和工业用途的重组蛋白当中。
蔡垚博士与合作者使用毕赤酵母成功表达出人H亚基铁蛋白(P-HFn)。通过仿生生物矿化的方法,首次使用P-HFn合成了磁性铁蛋白纳米颗粒,P-MHFn。P-MHFn磁性铁蛋白纳米颗粒具有超顺磁性和类过氧化物酶活性,具有较宽的pH耐受范围(pH5.0-11.0)。体内近红外荧光成像实验表明,Cy5.5标记的P-MHFn可有效地积累在肿瘤中。在SD大鼠上的急性毒性研究表明,剂量不超过20 mg Fe / kg体重时,动物的体重、血液学参数、生化指标及组织检查均无异常。表明P-MHFn磁性铁蛋白具有良好的生物医学应用价值。

图2:毕赤酵母表达的人H亚基铁蛋白用于磁性铁蛋白纳米颗粒的合成,荷瘤小鼠的近红外荧光成像。
该研究成果发表于Nanotechnology上。Cai, Y., Huang, J., Xu, H., Zhang, T. Cao, C., and Pan, Y. Synthesis, characterization and application of magnetoferritin nanoparticle by using human H chain ferritin expressed by Pichia pastoris. Nanotechnology. 2020, 31, 485709. DOI: 10.1088/ 1361-6528 / a bb15d
3. 肿瘤环境响应型介孔二氧化硅-人H亚基铁蛋白抗癌药物递送系统
化学疗法是大多数类型癌症常用的治疗方法,但是由于肿瘤细胞对化学疗法的抵抗性以及正常细胞非特异性摄取药物所引起的副作用,这种治疗方法的功效会受到严重限制。 建立安全高效治疗性化合物转运和释放的药物递送系统极为重要。HFn内部8纳米空腔可包裹运载药物,但HFn有限的内部空腔大小限制了装载药物分子的能力。介孔二氧化硅(MSN)具有多孔结构,可调节的孔径以及易于功能化的表面,可以包载大量不同类型的化合物分子。MSNs的化学稳定性高、尺寸均匀性好和固有低毒性。其较大的表面积可以附着不同的官能团,这些官能团可与靶向特定癌细胞类型的特定配体相结合。但在使用中要封堵MSN的孔道两端防止药物分子在非目标区域扩散出去,并且在载药的MSN到达目标区域后,当受到特定内部或外部刺激后需能够打开封堵剂,确保药物从MSN释放出来。
蔡垚博士与合作者成功设计和制备出基于MSNs和HFn的纳米药物递送平台,将HFn作为一种活性剂既充当封堵载抗癌药物分子的MSN孔上的刺激响应型“帽子”,又充当癌细胞上TfR1受体的靶向剂,此“二合一”功能简化了药物递送纳米颗粒的制备和优化。他们制备的氧化还原刺激响应型的纳米阀(释放药物的开关)是基于MSNs上修饰的化学物与HFn上的半胱氨酸之间的二硫键而形成的,二硫键被存在于细胞质中的还原剂(如谷胱甘肽)还原断裂,从而使得HFn脱落。 另外一种pH敏感型的纳米阀是基于MSNs上修饰的化学物的疏水基团和HFn的四相疏水通道之间的疏水作用而形成的,在溶酶体酸性条件下,由于质子化而降低了结合疏水作用,使得HFn脱落。在这两种纳米载体药物递送系统中,HFn均以高表面覆盖率与MSN偶联,并能有效地将荧光染料分子和阿霉素药物分子封堵在MSN孔中。与传统的环糊精封堵的MSN相比,MSN-HFn的药物释放效率更高。这两种纳米药物递送载体均能被PANC-1细胞有效吸收,并在胞吞后释放出药物,相比于传统的环糊精封堵的载药MSNs,它们能够更有效地杀死癌细胞,这与TfR1介导的MSN-HFn能更多的靶向肿瘤细胞有关。体内抗肿瘤效果评估实验研究显示出了MSN-HFn载药和递送具有优良治疗效果。
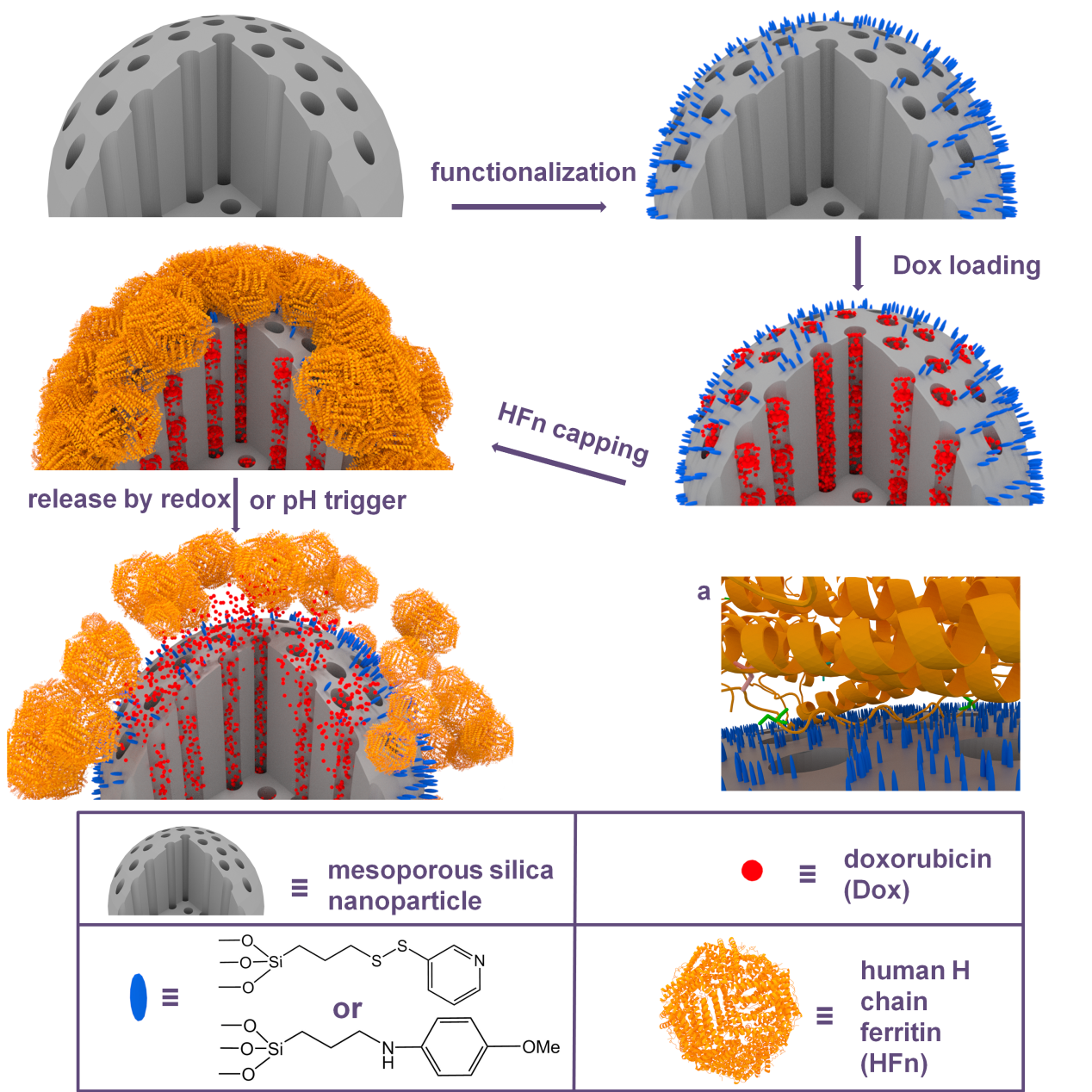
图3. 基于重组人H亚基铁蛋白和介孔二氧化硅纳米颗粒,成功设计和制备了一种新的靶向药物递送系统,该系统可响应肿瘤细胞内氧化还原电势的改变或pH值的改变而释放抗癌药物,并显示出在体内具有提高药物治疗癌症的效用。
该研究成果发表于Advanced Functional Materials上。Cai, Y., Deng, T., Pan, Y. and Zink, J.I. Use of ferritin capped mesoporous silica nanoparticles for redox and pH triggered drug release in vitro and in vivo. Advanced Functional Materials. 2020, 2002043. DOI: 10.1002 / adfm. 20200 2043.
https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.202002043
 当前位置:
当前位置: